همه چیز درباره ۳ واکسن کرونا که در ایران مجوز مصرف اضطراری گرفتند
واکسن های Strazenka-Oxford ، Kovacsine Bharat India و Sinofarm China سه واکسنی هستند که برای استفاده اضطراری در ایران تأیید شده اند ، بنابراین می توانند برای واکسیناسیون بیماری کرونا همراه با مطالعات تولید واکسن های داخلی در کشور و توسط موسسات مختلف وارد کشور شوند.
به گزارش مجله تفریحی زیباروز ، لازم به ذکر است که از زمان ابتلا به بیماری همه گیر Covid-19 و شیوع چالش برانگیز و جهانی این بیماری ، محققان و شرکت های داخلی و خارجی ایران در حال تولید واکسن برای این بیماری هستند. بر این اساس ، در میان شرکت های تولید کننده واکسن داخلی ، شرکت شفا فارمد در مجتمع دارویی برکت و موسسه رازی و همچنین مجتمع سپند وزارت دفاع وارد مرحله بالینی واکسن های کرونا شده است.
با بررسی تولید واکسن داخلی در کشور توسط موسسات مختلف ، واردات واکسن خارجی از شرکت های معتبر و کشورهای مورد تأیید سازمان بهداشت جهانی و تأیید اثربخشی آنها در آزمایشات بالینی ، بهترین روش برای کنترل بیماری همراه با سایر اقدامات پیشگیرانه در کشور.
بر این اساس ، با توسعه شرکت های داخلی برای تولید واکسن کرونا در مرزها ، سازمان غذا و داروی ایران واکسن Covid-19 را از سایر شرکت های خارجی معرفی کرده است. پس از واردات واکسن اسپوتنیکف روسی به عنوان اولین محموله واکسن کرونا به کشور و ادامه واردات در چندین فاز در کشور ، تعداد بسیار کمی از افراد واکسیناسیون بیماری Covid-19 انجام شده است.
مجوزهای ورود و مصرف مشروط قبلاً برای چندین واکسن وارداتی دیگر در کشور صادر شده است – از جمله واکسن Strazenka-Oxford از سایت های کره جنوبی SKBio و R-pharm روسیه ، واکسن آهنگر از Bharat Biotech India و واکسن BBIBP. -Cor V محصولات Sinofarm چین.
بر این اساس ، کمیته سازماندهی مطالعه Covid-19 در گزارشی به ارائه مشخصات واکسن های استرازنکا ، بهارات هند و سینوفرم ، که در ایران تصویب های اضطراری دریافت کرده اند ، پرداخت. این بروشور براساس آخرین داده های منتشر شده در مورد واکسن های اورژانسی تهیه شده و به صورت مشخصات واکسن ، پراکندگی استفاده و جزئیات مراحل مطالعات بالینی آنها منتشر شده است.
واکسن Strazenka-Oxford (دو سایت کره جنوبی SKBio و روسیه R-pharm)
این دو واکسن از دانشگاه آکسفورد و شرکت انگلیسی-سوئدی Strazenka است و براساس قرارداد استرازنکا با شرکت های کره ای و روسی تولید می شود.
واکسن استرازنکا-آکسفورد با همکاری موسسه R-pharm روسیه تولید می شود ، اما هنوز اطلاعاتی در مورد اثربخشی این واکسن منتشر نشده است.
واکسن Astrazenka-Oxford کره جنوبی است ، اما برای موارد اضطراری توسط سازمان بهداشت جهانی تأیید شده است و حدود 40 میلیون دوز برای استفاده خانگی در کره جنوبی تولید شده است. این واکسن در 15 فوریه 2021 توسط سازمان بهداشت جهانی برای استفاده اضطراری تأیید شد.
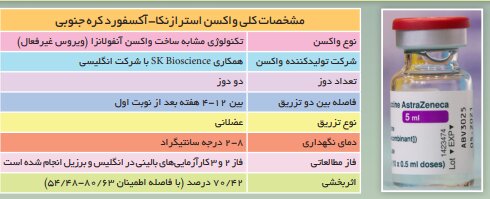
مشخصات عمومی واکسن Strazenka-Oxford در کره جنوبی
فناوری این واکسن مشابه فناوری واکسن آنفلوانزا است و ویروسی غیرفعال است که باید در دو دوز تزریق شود. فاصله زمانی بین دو تزریق بین چهار تا 12 هفته بعد از اولین دوز است و نوع تزریق عضلانی است.
واکسن باید در دمای دو تا هشت درجه سانتیگراد نگهداری شود. لازم به ذکر است که آزمایشات بالینی فاز 2 و 3 این واکسن در انگلستان و برزیل انجام شده و 70.42٪ موثر بوده است.
واکسن کوواکسین از بهارات بیوتک هند
این واکسن از ویروس کرونا ویروس غیرفعال و با همکاری شورای تحقیقات پزشکی (ICMR) و موسسه ملی ویروس شناسی هند (NIV) ساخته شده است.
این واکسن برای استفاده اضطراری در هند در تاریخ 3 ژانویه 2020 تأیید شده است. مطالعات بالینی نشان داده است که این واکسن از نظر ایمنی و اثر محافظتی قوی در مطالعات حیوانات بر روی همسترها و پستانداران غیر انسانی دارد.
همچنین نشان داده شده است که کووکسین در آزمایشات بالینی فاز 1 و فاز 2 آنتی بادی علیه Covid-19 تولید می کند.
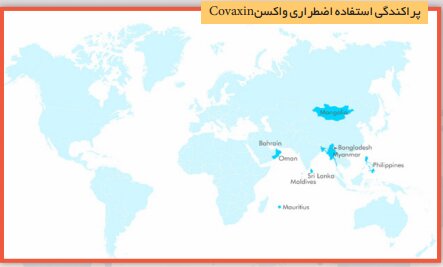
طبق گفته وزارت بهداشت ، این واکسن در هند و ایران تأیید شده است و در موارد اضطراری در مغولستان ، میانمار ، سریلانکا ، فیلیپین ، بحرین ، عمان ، مالدیو و موریس استفاده می شود.
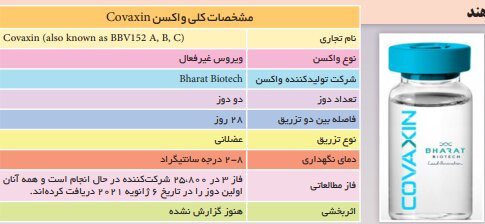
مشخصات عمومی کوواکسین
این واکسن نیز توسط ویروس غیرفعال می شود و توسط Bharat Biotech تولید می شود. این واکسن نیز در دو دوز تزریق می شود و فاصله بین دو تزریق 28 روز است و تزریق از طریق عضله انجام می شود. واکسن کوواکسین باید در دمای دو تا هشت درجه سانتیگراد نگهداری شود.
مرحله سوم واکسن بر روی 25،800 شرکت کننده در حال انجام است و همه در 6 ژانویه 2021 اولین دوز واکسن را دریافت کردند. باید در نظر داشت که هنوز اثربخشی این واکسن گزارش نشده است.
واکسن BBIBP-Cor V ساخت شرکت سینوفارم چین
این واکسن توسط انستیتوی محصولات بیولوژیکی پکن و شرکت دولتی Sinofarm در چین ساخته شده است.
این واکسن در 3 کشور امارات ، بحرین و چین و همچنین 19 کشور: بحرین ، کامبوج ، چین ، مصر ، مجارستان ، عراق ، اردن ، مراکش ، نپال ، پاکستان ، پرو ، صربستان ، سیشل ها ، امارات ، ایران ، تایید شده است. آرژانتین زیمبابوه ، گینه ، مناطق گرمسیری و جمهوری دموکراتیک خلق لائو واکسن اضطراری را تأیید کرده اند.
مشخصات عمومی Sinofarm
واکسن Sinofarm نیز از ویروس غیرفعال شده توسط شرکت چینی Sinofarm ساخته شده است. دوز این واکسن در دو دوز است و فاصله بین دو تزریق 21 روز است و تزریق به صورت عضلانی انجام می شود. واکسن باید در دمای دو تا هشت درجه سانتیگراد نگهداری شود.
مرحله سوم مطالعات این واکسن در حال انجام است و بدون انتشار یافته های مطالعه در مجلات است. اثربخشی Sinofarm در مطالعه چینی 34/79 و در مطالعه امارات متحده عربی 86 درصد بود.

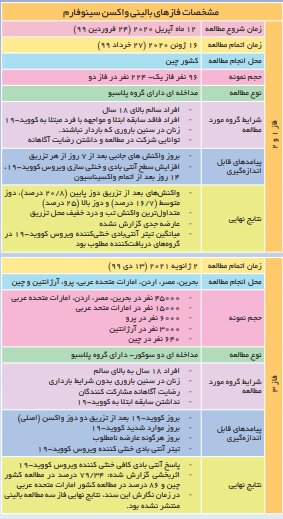
مشخصات فاز 1 و 2 بالینی Sinofarm
فازهای اول و دوم مطالعه بالینی Sinofarm در 12 آوریل 2020 آغاز شد و در 16 ژوئن 2020 به پایان رسید. سایت مطالعه در چین واقع شد و نمونه 96 نفر در مرحله اول و 224 نفر در مرحله دوم بود. نوع مطالعه مداخله ، گروه دارونما داشت.
شرایط گروه مطالعه شامل: افراد سالم بالای 18 سال ، افرادی که در طول تاریخ در معرض Covid-19 نبوده اند ، زنان در سن باروری که باردار نبوده اند و افرادی که ممکن است در این مطالعه شرکت کنند و رضایت آگاهانه برای شرکت در این مطالعه را داشته باشند.
پیامدهای قابل اندازه گیری در این دو مرحله عبارتند از: بروز واکنشهای جانبی 7 روز پس از هر تزریق ، افزایش سطح آنتی بادی و خنثی سازی ویروس Covid-19 14 روز پس از واکسیناسیون بود.
همچنین نتایج نهایی این دو مرحله شامل: واکنشهای بعد از تزریق دوز کم 20.8٪ ، دوز متوسط 16.7٪ و دوز بالا 25٪ ، شایعترین واکنش تب و درد خفیف در محل تزریق ، هیچ عارضه جدی مشاهده نشده و یک تیتر متوسط آنتی بادی برای خنثی سازی Covid-19 این ویروس در گروه های گیرنده مطلوب بود.
پایان مرحله سوم مطالعه بالینی واکسن Sinofarm به ترتیب در 2 ژانویه 2021 و 4 ژانویه 2017 بود. این مطالعه در بحرین ، مصر ، اردن ، امارات متحده عربی ، پرو ، آرژانتین و چین انجام شد و حجم نمونه در بحرین ، مصر ، اردن ، امارات متحده عربی 45000 ، در امارات 15000 ، در پرو 6000 ، در آرژانتین 3،000 و در چین 640 نفر بود. . نوع مطالعه مداخله ای دوسوکور بود – با یک گروه دارونما.
شرایط گروه مطالعه در مرحله سوم شامل افراد سالم بالاتر از 18 سال ، زنان در سن باروری بدون بارداری ، رضایت آگاهانه شرکت کنندگان و عدم سابقه Covid-19 بود.
در همان زمان ، عواقب قابل اندازه گیری در این مرحله ، بروز Covid-19 پس از دو دوز واکسن ، بروز موارد شدید Covid-19 ، بروز هرگونه عوارض جانبی و علامت گذاری آنتی بادی برای خنثی سازی ویروس Covid-19 ارزیابی شدند؛ پاسخ کافی به آنتی بادی هایی که ویروس Covid-19 را خنثی می کنند ، 34/79 درصد اثر را در مطالعه چینی و 86 درصد را در مطالعه امارات متحده عربی گزارش کرد.
طبق کمیته سازماندهی تحقیقات Covid-19 ، در زمان نگارش این مقاله ، نتایج نهایی مرحله سوم آزمایش بالینی واکسن منتشر نشده است.
طبق گفته وزارت بهداشت ، لازم به ذکر است که در 8 فوریه ، سازمان بهداشت جهانی واکسن Oxford-AstraZeneca که توسط کره جنوبی SKBio و واکسن Covaxin از Bharat Biotech India برای استفاده اضطراری در سراسر جهان تهیه شده است ، توصیه کرد. این سازمان باید با استفاده از واكسن اضطراری ، كیفیت ، ایمنی و اثر بخشی واكسن و همچنین شرایط و دستگاه های تهیه واكسن را مورد بررسی قرار دهد.
انتهای پیام